Allgemeine Chemie
Zeigt 1-4 von 4 Produkten 4 Produkte in Allgemeine Chemie
Filters
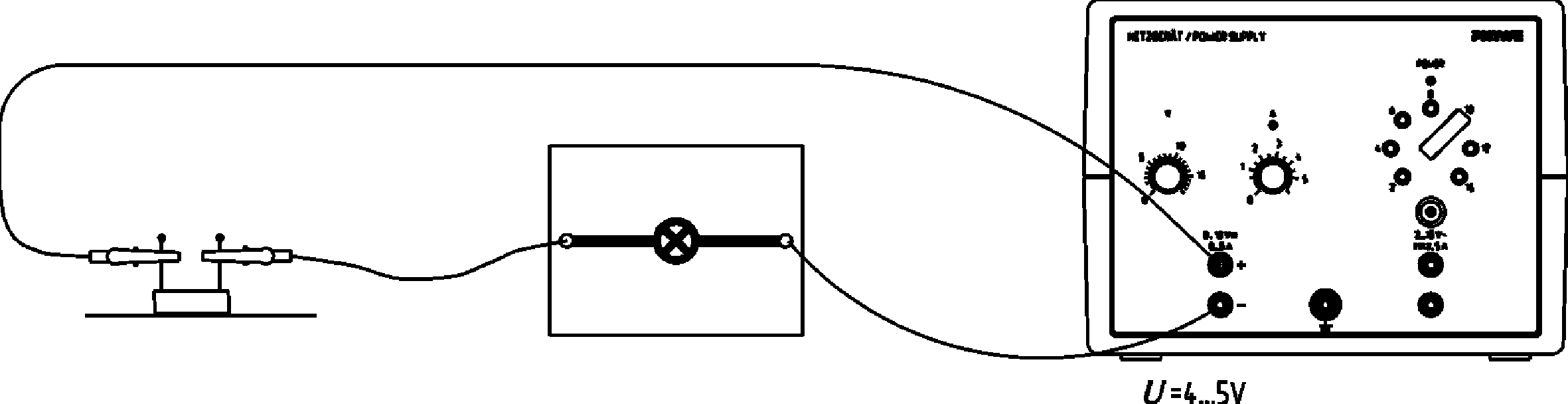
Eigenschaften von Lithium, Natrium und Kalium
Prinzip In diesem Versuch wird das Verhalten der Alkalimetalle an der Luft, sowie die Flammenfärbung bei deren Verbrennung untersucht. Die Reaktionsprodukte werden in Wasser gelöst, wobei der pH-Wert mit Hilfe des Indikators Phenolphtalein abgeschätzt wird. Abschließend wird die elektrische Leitfähigkeit der Alkalimetalle untersucht. Vorteile • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 2’239.20
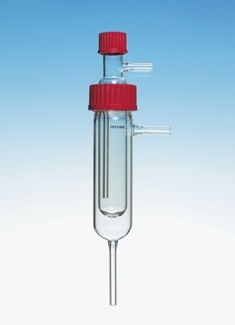
Gerät zur Gefrierpunkterniedrigung
Funktion und Verwendung Zur Bestimmung molarer Massen gelöster Stoffe durch Gefrierpunktserniedrigung (Kryoskopie). Das Gerät umfasst zwei zylindrische Glasgefäße, die ineinander gesetzt werden. Das äußere Gefäß besteht aus einem geschlossenen Glasrohr mit einer Glasgewindeverschraubung GL 45/32 und einem runden Boden. Das innere Gefäß ist ebenfalls geschlossen, hat aber einen flachen Boden. Am oberen Ende befindet sich eine Glasgewindeverschraubung GL 25/10. Unterhalb dieser Verschraubung befindet sich seitlich eine schräge Öffnung mit einer Glasgewindeverschraubung GL 18 mit Verschlusskappe. Zur Messung von Gefrierpunktserniedrigungen werden die beiden Gefäße ineinandergesetzt und dicht verschraubt. Das äußere Gefäß wird mit einer Flüssigkeit zum Wärmetransport (z. B. Ethanol) befüllt. Das innere Gefäß nimmt das ausgewählte Lösungsmittel auf. In der oberen Glasgewindeverschraubung wird ein Temperaturmessgerät (Thermometer oder elektronischer Thermosensor) befestigt. Das so zusammengesetzte Gerät wird in ein Behälter mit einer Kältemischung gehängt und der Gefrierpunkt des Lösungsmittel ermittelt. Eine zweite Gefrierpunktsbestimmung wird ausgeführt, nachdem zu dem Lösungsmittel im inneren Gefäß eine zu einer Pille gepresste Probe der zu untersuchenden Substanz zugegeben wurde. Aus der gemessenen Gefrierpunktserniedrigung und der Masse der zugegebenen Substanz kann die molare Masse dieser Substanz bestimmt werden.
CHF 330.05
Gerät zur Siedepunktserhöhung
Funktion und Verwendung Das Gerät dient zur Bestimmung molarer Massen gelöster Stoffe durch Siedepunktserhöhung (Ebullioskopie). Das Gerät umfasst zwei zylindrische Glasgefäße, die ineinander gesetzt werden. Das äußere Gefäß besteht aus einem Glasrohr mit einer Glasgewindeverschraubung GL 45/32, einem seitlichen Glasrohrstutzen direkt unterhalb der Verschraubung und einem Glasrohrstutzen am Boden. Das innere Gefäß ist unten geschlossen. Am oberen Ende befindet sich eine Glasgewindeverschraubung GL 25/10. Unterhalb dieser Verschraubung befindet sich seitlich eine Öffnung im Glasrohr, die in ein Glasröhrchen mündet, das bis kurz oberhalb des Gefäßbodens reicht. Zur Messung von Siedepunktserhöhungen wird das innere Gefäß dicht mit dem äußeren verschraubt. Das äußere Gefäß wird über den unteren Glasrohrstutzen mit dem Rundkolben verbunden. Der Rundkolben und das innere Gefäß werden mit dem für die Messung ausgewählten Lösungsmittel befüllt. In der Glasgewindeverschraubung des inneren Gefäßes wird ein Temperaturmessgerät (Thermometer oder elektronischer Thermosensor) befestigt. Das Lösungsmittel im Rundkolben wird mit einem Heizpilz zum Sieden erhitzt. Der Lösungsmitteldampf gelangt über den unteren Glasrohrstutzen in das äußere Gefäß und über die Öffnung dann in das innere Gefäß und erwärmt das sich dort befindende Lösungsmittel zum Sieden. Der Siedepunkt wird gemessen. Eine zweite Siedepunktbestimmung führt man aus, nachdem zu dem Lösungsmittel des inneren Gefäßes eine zu einer Pille gepressten Probe der zu untersuchenden Substanz zugegeben wurde. Aus der gemessenen Siedepunktserhöhung und der Masse der zugegebenen Substanz kann die molare Masse dieser Substanz bestimmt werden.
CHF 429.90
Periodensystem: ähnliche Eigenschaften der Elemente einer Hauptgruppe am Beispiel von Gruppe 2
Prinzip Chemische Elemente lassen sich aufgrund der in weiten Bereichen ähnlichen Eigenschaften in Gruppen zusammen fassen. Diese Elemente sind im Periodensystem waagrecht in Gruppen angeordnet. Diese Einordnung hat eine wichtige Bedeutung, so lassen sich aus den Eigenschaften der vorherigen Gruppenmitglieder voraussagen, welche grundlegenden Eigenschaften die folgenden Elemente der Gruppe besitzen. In diesem Schülerversuch werden die Elemente Magnesium und Calcium auf ihre Eigenschaften untersucht und bewiesen, dass Elemente der gleichen Gruppe chemisch ähnliche Eigenschaften zeigen. Vorteile • Einfache Versuchsdurchführung (keine teuren Geräte notwendig) • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 340.20


















 Versuche & Sets
Versuche & Sets