Chemische Kinetik
Zeigt 1-6 von 6 Produkten 6 Produkte in Chemische Kinetik
Filters
Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt- Reaktion) -
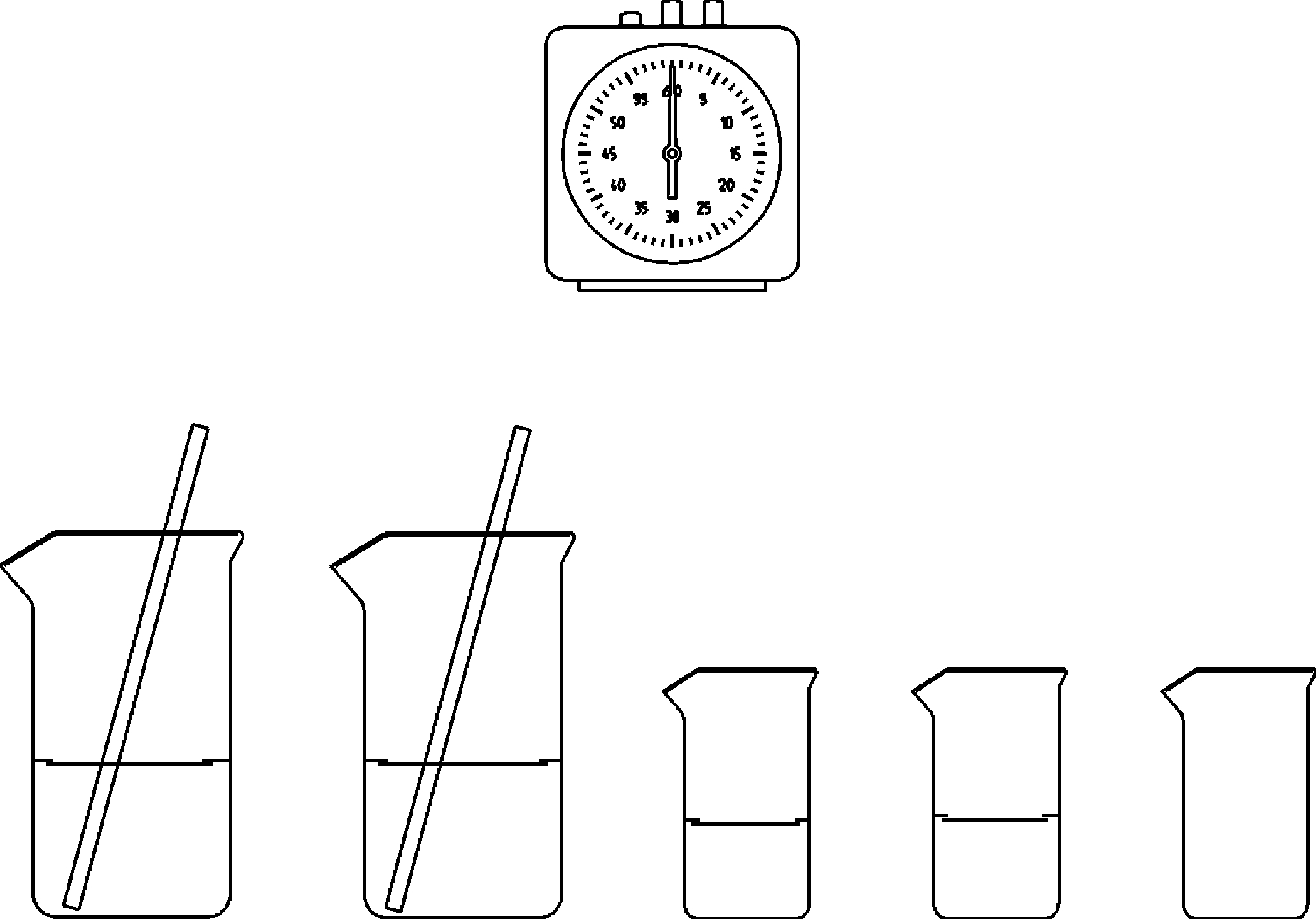
Prinzip Bei einer chemischen Reaktion ist die Reaktionsgeschwindigkeit u.a. abhängig von Reaktionstemperatur und Konzentration der beteiligten Stoffe. Dabei ist die Konzentration der Ausgangsstoffe einer der wesentlichen Einflussgrößen auf die Reaktionsgeschwindigkeit. Allgemein gilt dabei: Je höher die Konzentration der Ausgangsstoffe ist, desto schneller läuft die entsprechende Reaktion ab. Bei einfachen Reaktionen (erster Ordnung) ist die Reaktionszeit umgekehrt proportional zur Konzentration der Ausgangsstoffe. Vorteile • Didaktisch anschauliche Einführung in die Kinetik chemischer Reaktionen • Versuchsdurchführung gemäß Richtlinien für Sicherheit im Unterricht (Gefährdungsbeurteilung verfügbar)
CHF 1’105.50
Reaktionsgeschwindigkeit und Aktivierungsenergie für die saure Hydrolyse von Essigsäureethylester
Prinzip Essigsäureethylester wird in saurer Lösung nach einem Zeitgesetz pseudo-erster Ordnung zu äquivalenten Mengen an Ethanol und Essigsäure hydrolysiert. Durch alkalimetrische Bestimmung der gebildeten Essigsäure kann auf die zeitliche Konzentration an Ester geschlossen werden. Vorteile • Thermostat für präzise Temperaturkontrolle • Stabiler und sicherer Aufbau durch solides Stativmaterial
CHF 3’488.65
Abhängigkeit der Reaktionsgeschwindigkeit von der Stoffart
Prinzip Nach den fundamentalen Gesetzen der Chemie läuft eine chemische Reaktion dann spontan ab, wenn sie exotherm ist, d.h. Energie (meist in Form von Wärme) an die Umgebung abgibt. Die Reaktionsgeschwindigkeit einer Reaktion ist dabei abhängig von der Reaktionstemperatur und die Konzentration der Ausgangsstoffe (eine Erhöhung der Reaktionstemperatur bzw. der Konzentration der Ausgangsstoffe führt zu einer Erhöhung der Reaktionsgeschwindigkeit). Dieser Versuch soll zeigen, dass bei gleicher Temperatur, gleicher Konzentration und vergleichbarer Oberfläche der Ausgangsstoffe trotzdem ein Unterschied in der Reaktionsgeschwindigkeit bei vergleichbaren "Reaktionsmechanismen" beobachtbar ist. Dazu wird Magnesium bzw. Zink mit konzentrierter Salzsäure zur Reaktion gebracht und die entstandene Menge an Wasserstoff untersucht. Beide Reaktionen laufen nach dem gleichen Schema ab ("Metall + Säure -> Salz + Wasserstoff") und dennoch wird eine unterschiedliche Reaktionsgeschwindigkeit beider Reaktionen beobachtet (anhand der Menge an gebildeten Wasserstoff). Obwohl die Reaktionstemperatur, Ausgangskonzentration und Oberfläche der Ausgangsstoffe in etwas gleich ist, läuft die Umsetzung von Magnesium mit Salzsäure deutlich schneller ab. Aufgrund der Stellung in der elektrochemischen Reihe der Elemente hat Magnesium gegenüber Wasserstoff ein wesentlich negativeres Potential als Zink. Dadurch reagiert Magnesium heftiger, d. h. schneller mit Salzsäure reagieren als Zink. Vorteile • Anschauliche Einführung in Kinetik chemischer Reaktionen • Versuchsdurchführung gemäß den Richtlinien für Sicherheit im Unterricht (Gefährdungsbeurteilung verfügbar)
CHF 4’131.20
Kinetik der Inversionsreaktion von Saccharose
Prinzip Vorteile • Einfacher Einstieg in die Polarimetrie • Verbindung von methodischen Fähigkeiten und theoretischem Wissen Die durch Hydronium-Ionen katalysierte Inversionsreaktion von Saccharose liefert Invertzucker, ein Gemisch aus Glucose und Fructose. Der Reaktionsverlauf wird von einer Änderung des Drehwinkels für polarisiertes Licht begleitet. Während Glucose rechtsdrehend ist, dreht Invertzucker die Polarisationsebene linear polarisierten Lichts nach links. Die zeitliche Änderung des Drehwinkels von polarisiertem Licht wird mit Hilfe eines Halbschattenpolarimeters gemessen.
CHF 4’402.-
Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur (Essigsäure - Magnesium - Reaktion)
Prinzip Die Geschwindigkeit einer chemischen Reaktion wird stark von der Temperatur beeinflusst. Durch die Umsetzung von Magnesium mit Essigsäure bei verschiedenen Temperaturen und Messen der dabei jeweils pro Zeiteinheit gebildeten Mengen an Wasserstoff lässt sich dies gut zeigen. Ein Vergleich der Anfangsgeschwindigkeiten der Reaktionen zeigt in erster Näherung etwa eine Verdopplung der Reaktionsgeschwindigkeit bei einer Temperaturerhöhung um 10 K. Vorteile • Didaktisch anschauliche Einführung in die Kinetik chemischer Reaktionen • Gefährdungsbeurteilung verfügbar - einfache und schnelle Versuchsvorbereitung
CHF 4’520.95
Maxwellsche Geschwindigkeitsverteilung
Prinzip Die Moleküle eines Gases bewegen sich mit unterschiedlichen Geschwindigkeiten. Im Modellversuch mit dem Gerät zur kinetischen Gastheorie kann diese Verteilung durch Auffangen von Kugeln auf der Platte mit Ringsektoren veranschaulicht werden. Das Sammeln dieser Kugeln mit dem Auffänger mit Registrierkammer ergibt die Häufigkeitsverteilung der Geschwindigkeiten (Maxwellsche Verteilung). Vorteile • Gleichermaßen als Praktikums- und Demonstrationsversuche geeignet • Einzigartiger Versuch zur quantitativen Untersuchung der kinetischen Gastheorie • Mit ausführlicher Versuchsliteratur • „Visualisierung“ der Maxwell Boltzmann Verteilung
CHF 6’647.55


















 Versuche & Sets
Versuche & Sets