Anorganische Chemie
Zeigt 1-10 von 10 Produkten 10 Produkte in Anorganische Chemie
Filters
Bindung von Stickstoff durch unedle Metalle
Prinzip In diesem Versuch wird die Reaktivität von Stickstoff mit verschiedenen Metallen untersucht. Stickstoff als ein typisches Nichtmetall sollte mit (unedlen) Metallen zu dem entsprechenden Salz in Form einer exothermen Reaktion reagieren. Dennoch reagieren Metalle kaum mit Stickstoff, so reagiert Stickstoff bei Zimmertemperatur nur mit sehr unedlen Metallen (Alkalimetalle wie Lithium) zu den entsprechenden Nitriden. Dies liegt dran, dass Stickstoff (elementar) immer als Molekül vorkommt. Die Stickstoffatome sind dabei in dem Stickstoffmolekül durch drei bindende Elektronenpaare miteinander verbunden. Die Dreifachbindung zwischen beiden Stickstoffatomen ist eine unpolare Atombindung. Daher ist die Stickstoff-Dreifachbindung aufgrund der unpolaren Dreifachbindung außerordentlich reaktionsträge. Dennoch ist es aber möglich, dass Stickstoff mit unedlen Metallen (z.B. Calcium oder Magnesium) reagiert, wie in dem Versuch gezeigt wird. Vorteile • Einfacher Versuchsaufbau, der zeigt, dass auch reaktionsträger (molekularer) Stickstoff mit Metallen reagiert. • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 747.35
Chemische Springbrunnen
Prinzip Einige Gase wie Chlorwasserstoff lösen sich sehr gut in Wasser. So löst 1 Liter Wasser bei 20 °C ca. 443 Liter Chlorwasserstoff. In einem geschlossenen Kolben bildet sich bei Kontakt des Gases mit etwas Wasser rasch ein Unterdruck, da sich das Gas im Wasser löst und weiteres Wasser in den Kolben gesaugt wird. Darauf beruht die Funktion des chemischen Springbrunnens, eine spannende Art, die Löslichkeit von Gasen in Wasser zu demonstrieren. In der hier gezeigten Variante wird in ein und derselben Apparatur der Chlorwasserstoff erzeugt, der Kolben des Springbrunnens damit gefüllt und der Brunnen zum Sprudeln gebracht. Vorteile • Anschaulicher Versuch, der die extreme Löslichkeit von Chlorwasserstoff in Wasser verdeutlicht und zugleich eindrucksvoll das Entstehen von Unterdruck (Prinzip chemischer Springbrunnen) zeigt • Schnelle und einfache Versuchsvorbereitung (Versuchsanleitung und Gefährdungsbeurteilung verfügbar)
CHF 1’820.30
Eigenschaften des Aluminiums
Prinzip In diesem Versuch werden die Eigenschaften von Aluminium untersucht. Dazu wird Aluminiumpulver entzündet, das Reaktionsverhalten von Aluminium gegenüber Salzsäure sowie der pH-Wert einiger Aluminiumsalze untersucht. Vorteile • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 3’692.40
Erzsammlung für Röntgenfloureszenzanalyse, 50 Stück
Funktion und Verwendung 40 ausgesuchte Roherze zur Metallerzeugung. Auswahl besonders reichhaltiger Erzstücke.
CHF 394.45
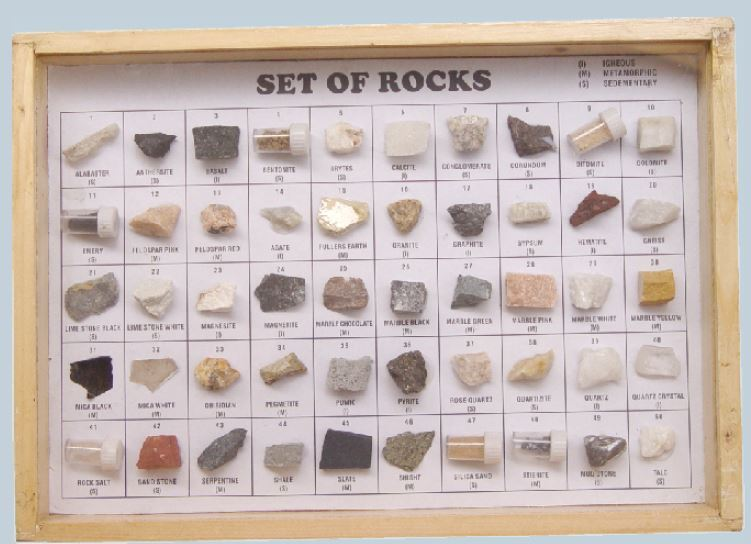
Erzsammlung, 40 Stück
Funktion und Verwendung 40 ausgesuchte Roherze zur Metallerzeugung. Auswahl besonders reichhaltiger Erzstücke.
CHF 433.10
Komplexsalze
Prinzip In diesem Versuch untersuchen die Schüler die Bildung einer Komplexverbindung. Dabei erkennen Sie, dass bei vielen Metallionen von Nebengruppenelementen bereits in wässriger Lösung eine Komplexverbindung vorliegt. Das Zentralion umgibt sich dabei mit einer Hydrathülle (Wasser-Moleküle als Liganden um das Zentralion), man spricht auch von einem aquotisierten Metallion. Die Schüler beobachten anhand der Farbänderung der Verbindungen, dass Komplexbildungsreaktionen Gleichgewichtsreaktionen sind und daher der Ammoniak den Wasser-Liganden am Kupferion ersetzen kann. Beim Isolieren des Ammoniak-Komplexes stellen die Schüler fest, dass auch vermeintlich stabile Komplexe "einem" Komplexzerfall unterliegen. Vorteile • Anschauliche Einführung in das Themengebiet "Komplexchemie" • Versuchsdurchführung gemäß den aktuellen Vorschriften (Gefährdungsbeurteilung verfügbar)
CHF 620.80
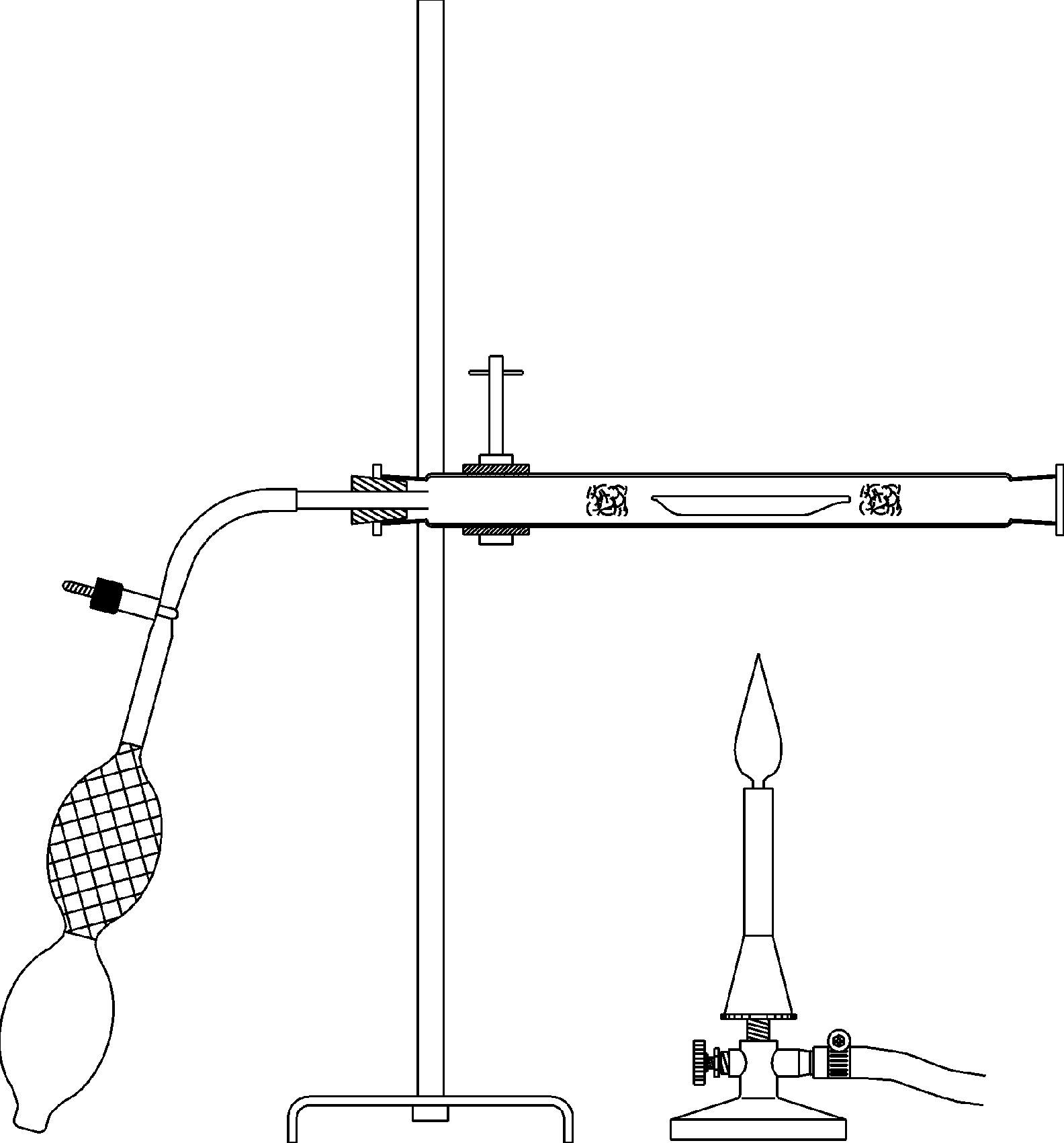
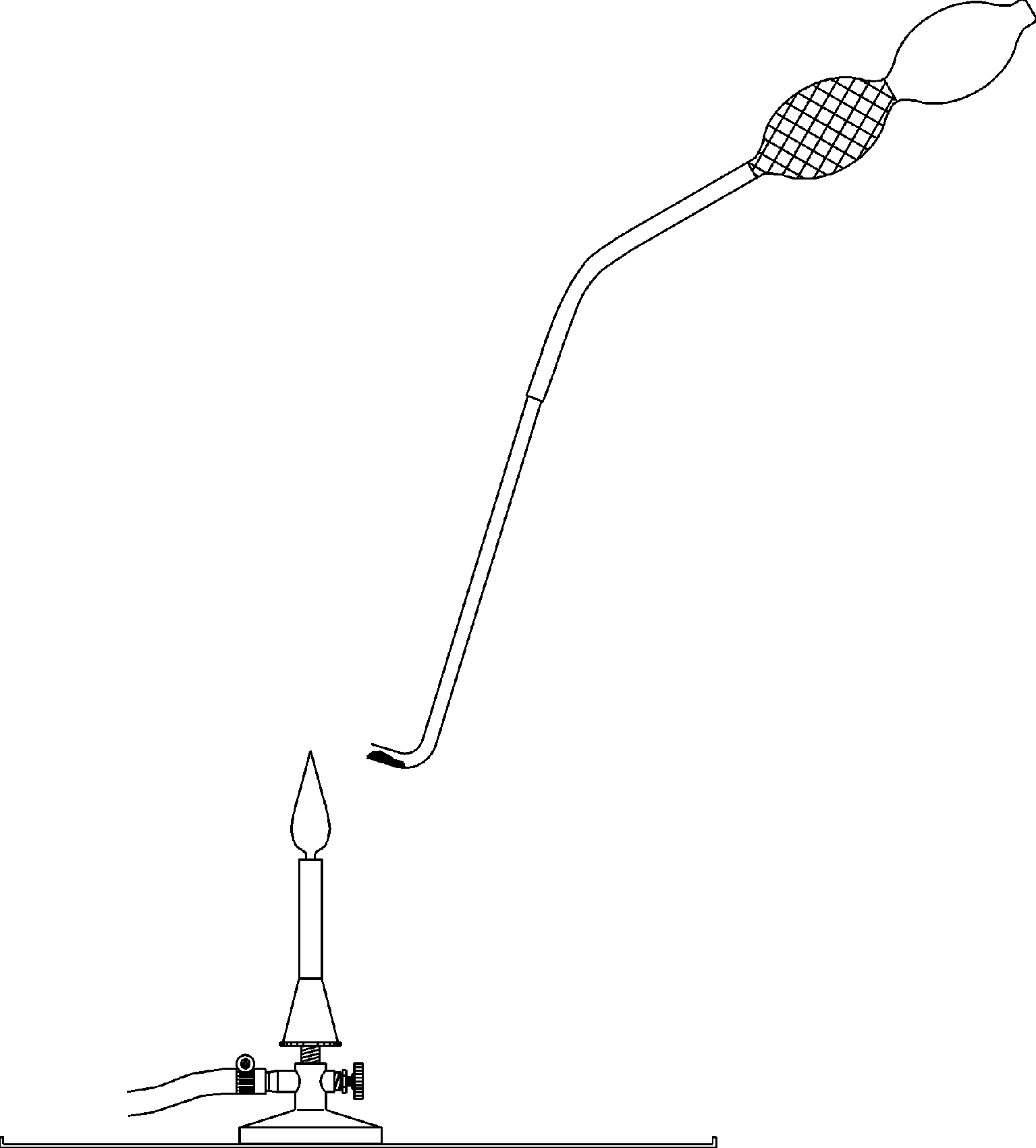
Luft - ein Gemisch aus den Gasen Sauerstoff und Stickstoff
Prinzip In diesem Versuch wird die chemische Zusammensetzung von Luft untersucht. Hierfür wird festes Kupfer in Gegenwart von Luft erhitzt. Kupfer verbindet sich beim Erhitzen mit dem Sauerstoff der Luft zu Kupferoxid. Führt man diese Reaktion in einer geschlossenen Apparatur mit einem abgemessenen Luftvolumen durch, so erhält man Aufschluss über den Sauerstoffgehalt der Luft. Vorteile • Einsatz als fachübergreifender Versuch möglich • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 4’185.45
Reaktion von Magnesium und Calcium mit Wasser - Hydroxidbildung -
Prinzip In den Experimenten werden aus der Gruppe der Erdalkalimetalle Calcium und Magnesium mit ihrer großen Reaktionsfähigkeit vorgestellt. Die vorliegenden Versuche zeigen die Reaktion mit Wasser unter Hydroxidbildung. Vorteile • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 3’118.-
Saure, neutrale und alkalische Reaktionen von Salzlösungen
Prinzip Im Allgemeinen lässt sich aus der Stärke bzw. Schwäche der Säuren und Basen, aus welchen die Salze hergestellt wurden, der pH-Wert ableiten. Salze aus gleich starken Säuren und Basen (z.B. NaCl) reagieren in wässriger Lösung neutral. Wohingegen Salze aus einer schwachen Säure/Base sowie starken Base/Säure entweder alkalisch oder sauer reagieren (z.B. reagiert Natriumacetat aus schwacher Essigsäure und starker Natronlauge alkalisch). Vorteile • Zusammenhang zwischen Zusammensetzung einer Salzlösung und dem pH-Wert der Lösung wird anschaulich vermittelt • Experimentierliteratur für Schüler und Lehrer erhältlich: Minimale Vorbereitungszeit • Gefährdungsbeurteilung für Schüler und Lehrer erhältlich • Einfaches Lehren und effizientes Lernen beim Einsatz der verfügbaren interaktiven Experimentier-Literatur
CHF 494.30
Schmelzflusselektrolyse
Prinzip Die Schmelzflusselektrolyse von Natriumchlorid zur Gewinnung von Chlor und Natrium, das zu Natronlauge weiterverarbeitet wird, ist ein wichtiges großtechnisches Verfahren. Mit dem hier gezeigten Experiment kann man die bei diesem Verfahren wichtigen Schritte in einfacher Weise demonstrieren. Dabei wird aber aufgrund des hohen Schmelzpunktes von Natriumchlorid das niedriger schmelzende Bleichlorid als Modellsubstanz eingesetzt.
CHF 6’370.30


















 Versuche & Sets
Versuche & Sets